Khái quát các loại phản ứng của Toluen
Phản ứng của toluen được sắp xếp theo thứ tự dễ tham gia phản ứng thế, khó tham gia phản ứng cộng và bền vững với các loại phản ứng oxi hoá

Toluene đặc trưng bởi các phản ứng thế thơm điện di (hay còn gọi là phản ứng thế vào nhân thơm) tương tự như các hydrocacbon thơm thông thường.
Dung môi toluene là gì? 5 công dụng hữu ích của Toluene
Toluene có khả năng giải phóng electron lớn hơn so với các nguyên tử hydro ở cùng một vị trí do nhóm metyl (CH3) có trong nó. (xem phần phản ứng brom hoá và phản ứng của toluen với Cl2).
Trong phản ứng thế vào nhân thơm ta thường gặp hai tác nhân quan trọng là halogen (Br và Cl) có xúc tác bột Fe ở nhiệt độ cao và phản ứng thế nitro (với hỗn hợp HNO3 và H2SO4 đậm đặc nóng).
So với benzen, metyl ưa điện hơn. Với sự có mặt của FeCl3, Toluen bị clo hóa bởi Cl2 bằng phản ứng sulfo hóa nhân thơm để tạo ra axit sulfonic chlorotoluene (4-Chlorotoluene-3-sulphonic acid).
Phản ứng sulfo hóa nhân thơm tạo ra các đồng phân para- và ortho của chlorotoluene.
Một yếu tố quan trọng ảnh hưởng đến khả năng oxy hóa của toluene là chuỗi bên methyl của nó. Benzaldehyde (C6H5CHO) được sản xuất bằng cách kết hợp hợp chất với thuốc tím (KMNO4) và chromyl clorua (CrO2Cl2).
Bây giờ, hãy cùng phân tích chi tiết về các phản ứng đặc trưng của toluen
1. Phản ứng Brom hóa Toluen
Phản ứng halogen hoá brom cũng có thể gọi là phản ứng brom hóa toluen bằng HBr và H2O2 bằng cách sử dụng ánh sáng và HBr.
Phản ứng của toluen với brom được gọi là brom hóa toluen. Quá trình brom hóa của nó có thể diễn ra ở chuỗi bên hoặc vòng thơm. Điều kiện để xảy ra phản ứng giữa toluen và brom chỉ khi ta bẻ phân tử brom thành hai nguyên tử brom:
Br2 + to → Br +Br
Sau đó, nguyên tử brom có thể lấy một hydro từ toluen để tạo thành HBr
C6H5CH3 + Br → [C6H5CH2] + HBr
Gốc toluen được hình thành theo cách đó sẽ nhận brom để tạo thành sản phẩm:
[C6H5CH2] + Br2 → C6H5CH2Br + Br
a. Cơ chế gốc tự do
Nếu bạn đun hỗn hợp đủ nóng, brom sẽ phân tách thành các nguyên tử, nhưng nếu bạn sử dụng bước sóng ánh sáng thích hợp, bạn có thể thực hiện phản ứng ở nhiệt độ phòng.
Vì vậy, bạn có thể chạy phản ứng giữa toluen và brom với điều kiện cần và đủ là ánh sáng, hoặc bạn cũng có thể chạy nó trong bóng tối nếu bạn đun nóng hỗn hợp (cơ chế gốc tự do).
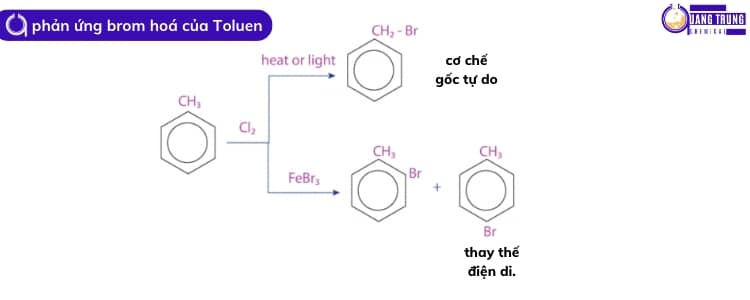
b. Phản ứng thế thơm điện di của toluen
Phản ứng thế thơm điện di của toluen bằng brom không xảy ra khi không có chất xúc tác thích hợp (chẳng hạn như AlCl₃ hoặc Fe) và nhóm metyl (CH3) không bị thay thế triệt để bằng brom vì không có tia cực tím để bắt đầu phản ứng.
Sản phẩm thu được từ phản ứng của toluen với brom có mặt chất xúc tác là bột sắt (Fe) sẽ là hỗn hợp của bromotoluene (CH3C6H4Br) chủ yếu là ortho và para.
Toluene có làm mất màu dung dịch brom không?
Cả Benzen và Toluene đều làm mất màu dung dịch brom.
2. Phản ứng của toluen với Cl2
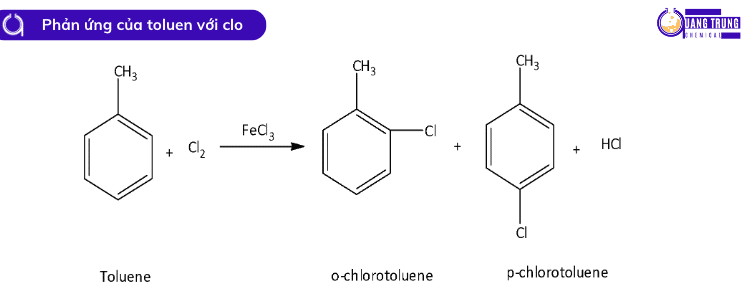
Trong phản ứng của toluen với clo khi có mặt sắt clorua, sản phẩm chính được tạo thành là o-clotoluen và p-clorotoluen.
Toluene phản ứng với Cl2 với sự có mặt của sắt clorua (FeCl3), sự thay thế vòng thơm điện di bằng Cl2 sẽ xảy ra chủ yếu ở vị trí para. Nó tạo ra sản phẩm là o-chlorotoluene và para-toluene và axit HCL. Các sản phẩm chính được hình thành trong phản ứng này là o-chlorotoluene và p-chlorotoluene.
Vì nhóm metyl gắn ở vòng ở vị trí para và ortho nhiều hơn so với vị trí meta, nên các phản ứng thế thơm điện di dễ dàng xảy ra ở những vị trí này (quy luật thế ở vòng benzen).
Chúng ta có thể viết phản ứng hóa học là:
Toluen phản ứng với clo khi có ánh sáng tạo thành
Toluen phản ứng với clo khi có ánh sáng tạo thành C6H5CH2Cl benzyl clorua. Phương trình phản ứng được viết là:
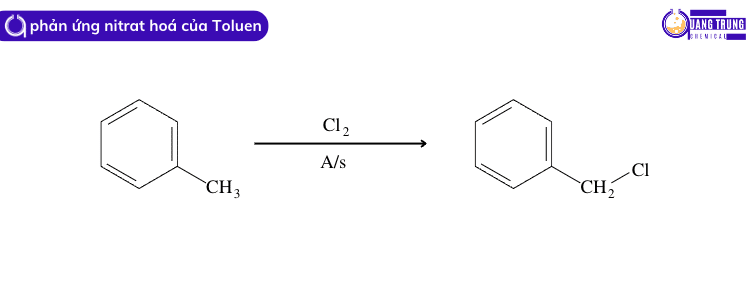
- Đây là một ví dụ điển hình của phản ứng quang hóa – phản ứng do ánh sáng mang lại.
- Sản phẩm hữu cơ là chloro metyl benzen.
Phản ứng của toluen với clo khi có ánh sáng được coi là phản ứng thế gốc tự do. Vì một trong những nguyên tử hydro trong nhóm metyl đã được thay thế bằng nguyên tử clo
Lưu ý: Chúng ta phải nhớ rằng nếu toluene phản ứng với clo mà không có chất xúc tác, sản phẩm sẽ là trichloromethylbenzene.
Trong trường hợp này, phản ứng của toluen với Cl2 mà không có chất xúc tác sự thay thế sẽ diễn ra ở nhóm methyl chứ không phải ở vòng. Sự có mặt của nhóm định hướng ortho và para chỉ tạo ra một cation ổn định khi các nhóm thế vào vị trí ortho và para đối với nhóm thế đã có mặt.
3. Phản ứng oxy hóa Toluen
Phản ứng oxi hoá của toluen để sản xuất axit benzoic
Vì toluene là một hợp chất thơm nên nó ít bị phản ứng oxy hóa hơn. Nhóm metyl của toluen là một chuỗi bên trong cấu trúc vòng thơm và bị oxi hóa thành nhóm cacboxyl khi có mặt chất oxi hóa mạnh.
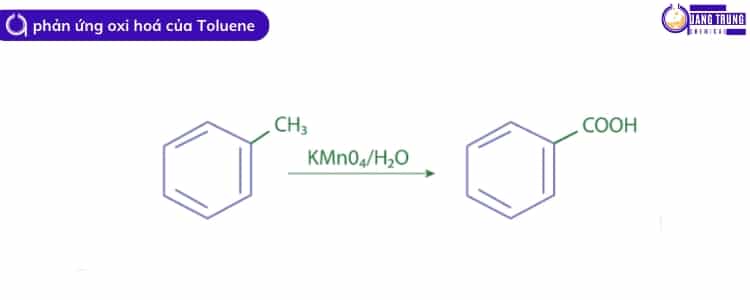
Phản ứng chính trong Hình 2 này là phản ứng của toluene với oxy trên chất xúc tác KMnO4 để tạo ra axit benzoic và nước, phản ứng tỏa nhiệt.
Quá trình oxy hóa toluene tạo thành benzaldehyde, chất này có thể tiếp tục bị oxy hóa để tạo thành axit benzoic. Chất trung gian dùng để tăng tốc độ phản ứng là KMnO4.
Cách nhận biết benzen với toluen
Phản ứng của toluen với dung dịch KMnO4 điều kiện xảy ra phản ứng là to còn được coi là phản ứng dùng để nhận biết benzen với toluen vì:
Toluen làm mất màu dung dịch KMnO4 trong khi benzen thì không có hiện tượng gì xảy ra.
2KMnO4 + C6H5CH3 + to→ H2O + KOH + 2MnO2 + C6H5COOK
4. Phản ứng Nitro hóa Toluen
Phản ứng nitro hoá toluen liên quan đến phản ứng thế vòng thơm điện di. Nó liên quan đến việc bổ sung nitrat ở vị trí ortho và meta của một hợp chất thơm.
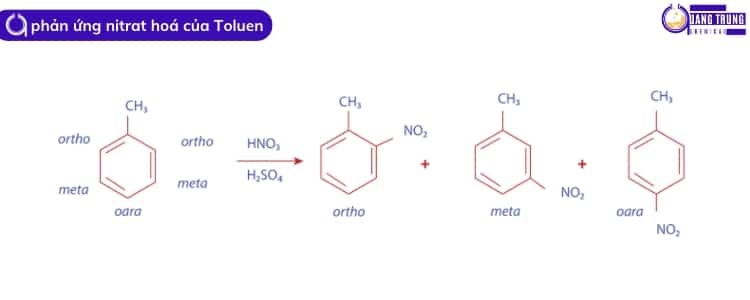
Việc đưa một nhóm nitro vào toluene tạo thành ortho-toluene & para-toluene và phản ứng được gọi là nitrat hóa toluene.
Phản ứng tuân theo cơ chế phản ứng thế điện di, và hỗn hợp axit sunfuric (H2SO4 đặc nóng) và axit nitric (HNO3) đậm đặc hoạt động như một tác nhân nitrat hóa.
Trong trường hợp này, axit sunfuric đậm đặc đóng vai trò là chất xúc tác và tạo ra ion nitronium hoạt động như một chất điện di.
Các ion nitronium (chất điện di) tấn công vào các vòng thơm, chủ yếu ở các vị trí ortho và para, nơi tiếp tục hình thành các sản phẩm ortho và para.
Do sự hiện diện của một nhóm metyl trên vòng toluene, quá trình nitrat hóa toluene nhanh hơn khoảng 25 lần so với benzen. Vì nhóm thế metyl đang kích hoạt đối với các nhóm định hướng -ortho và -para, do đó quá trình nitrat hóa toluen tạo ra các sản phẩm nitro thay thế nhiều.
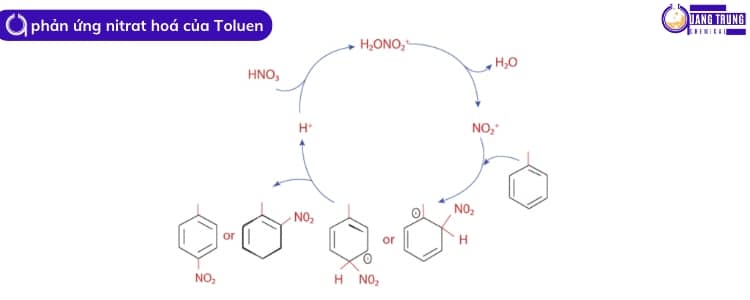
Tuy nhiên, việc sử dụng nhiệt độ thấp có thể ngăn chặn sự thay thế của nhiều hơn một nhóm nitro trên vòng thơm.
Ghi chú:
Trong điều kiện bình thường, toluene tạo ra cả ba đồng phân, trong đó tạo thành dẫn xuất ortho khoảng 63% và 34% sản phẩm phụ và 3% sản phẩm meta được tạo thành.
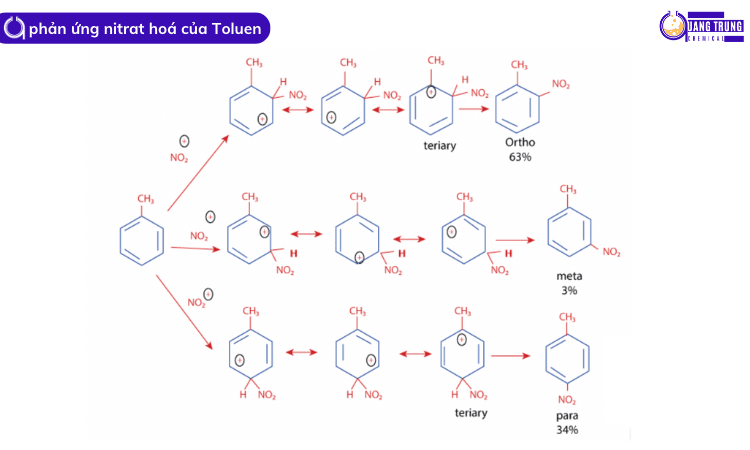
Năng suất cao của các sản phẩm ortho có thể được giải thích bằng cấu trúc cộng hưởng của ion areni hình thành như một chất trung gian.
Điều chế Toluene trong công nghiệp

Điều chế Toluene từ than đá
Phần dầu nhẹ của hắc ín than đá là nguồn chính để điều chế toluene thương mại. Phần dầu nhẹ được rửa bằng conc. H2SO4 để loại bỏ các bazơ có trong nó, sau đó loại bỏ các chất có tính axit bằng NaOH và cuối cùng là bằng nước.
Quy trình điều chế toluene từ than đá, sau khi được làm sạch phần dầu nhẹ được chưng cất phân đoạn. Hơi thu được trong khoảng 80 – 110 oC là 90% benzol, nó chứa 70 – 80% là benzen và 14 – 24% toluene. 90% benzol được chưng cất lại (trong khoảng 108 – 110 oC) để thu về toluen.
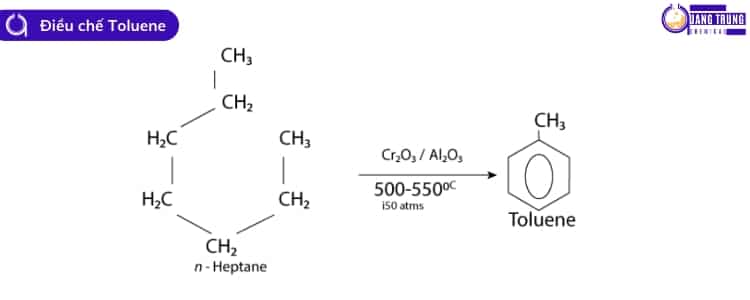
Điều chế Toluene từ Methylcyclohexane và N-Heptan
Điều chế toluene từ Methylcyclohexane và N-Heptan bằng cách tuần hoàn n-heptan với chất xúc tác Pt/Cr2O3 / Al2O3. Sau đó là quá trình aromat hóa.
Câu hỏi thường gặp
Toluene có phản ứng với nhựa không?
Toluene không phản ứng với nhựa. Tuy nhiên, nó là một dung môi tốt cho nhiều loại nhựa và có thể hòa tan nhiều loại nhựa thông thường.
Toluen có phản ứng với brom không?
Toluene phản ứng với brom khi có ánh sáng tạo ra benzyl bromide, trong khi với FeBr3, nó tạo ra p−bromotoluene.
Toluene có phản ứng với NaOH không?
Các ankylaren đơn giản như Toluen và Benzen là những chất không phản ứng với NaOH nguyên chất, nó không đủ mạnh để làm bazơ.
Tài liệu tham khảo
Tài liệu wikipedia về toluen



