Hydrocacbon thơm là gì?
Hydrocacbon thơm là các hợp chất hữu cơ có cấu trúc tròn chứa các liên kết sigma cùng với các điện tử pi được định vị. Chúng còn được gọi là arenes hoặc aryl hydrocarbon.
Giải thích về Hydrocacbon thơm chi tiết nhất
Hiđrocacbon thơm là “ hiđrocacbon không no có một hoặc nhiều vòng sáu cacbon (vòng benzen), trên đó các nguyên tử hydro được gắn vào mỗi nguyên tử C. Độ dài các liên kết C-C bằng nhau, độ dài các liên kết C-H cũng như nhau” .
Nhiều hydrocacbon thơm chứa vòng benzen (còn được gọi là vòng thơm). Vòng benzen được ổn định bằng cộng hưởng và các electron pi được định vị trong cấu trúc vòng.
Một vài ví dụ về hydrocacbon thơm được cung cấp dưới đây. Có thể quan sát thấy rằng tất cả các hợp chất này đều chứa một vòng benzen.
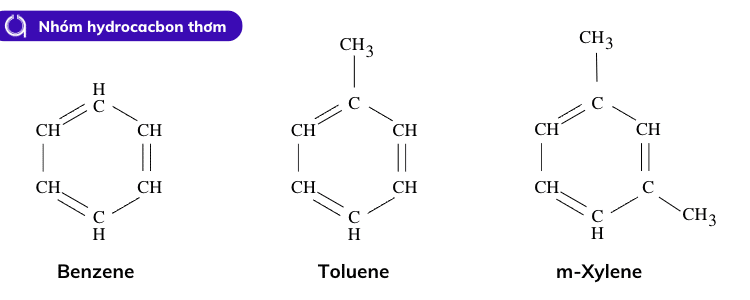
Kiểm tra ⇒ o-Xylen là gì? Tính chất, công dụng & phương pháp điều chế o Xylen
Quy tắc đọc tên của hydrocacbon thơm.
Cách đọc tên của hydrocacbon thơm đơn giản chứa sáu nguyên tử carbon được gọi là benzen. Tất cả các cấu trúc thay thế sáu thành viên khác được coi là dẫn xuất của benzen.
- Sáu nguyên tử cacbon của vòng benzen được đánh số từ 1 đến 6.
- Vị trí 1,4 gọi là vị trí para.
- Vị trí 2,6 được gọi là vị trí ortho.
- Vị trí 3,5 được gọi là vị trí meta.
- Trong hệ thống tên chung, các từ (o-) ortho, (p-) para và (m-) meta được sử dụng.
- Trong hệ thống tên danh pháp IUPAC, các số từ 1 đến 6 mà các nhóm thế được đính kèm sẽ được sử dụng.
- Các nhóm thế được đánh số theo thứ tự ưu tiên. Ví dụ được hiển thị trong sơ đồ.
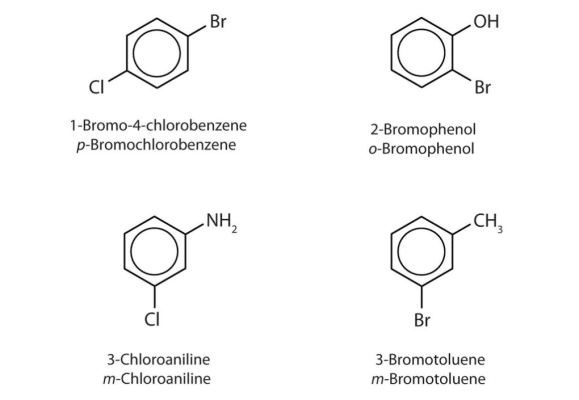
Tính chất của Hydrocacbon thơm
“Hợp chất đầu tiên được phân loại là hydrocacbon thơm là benzen”. Benzen là một hợp chất thơm có công thức hóa học C6H6.
Nó cũng là hydrocacbon phức tạp nhất. Mỗi nguyên tử carbon thuộc vòng benzen có hai liên kết sigma carbon-carbon, một liên kết sigma carbon-hydro. Kết quả là
Số lượng liên kết sigma = 6 × 2 ⇒ 12
Để tạo liên kết pi, cứ hai nguyên tử cacbon sẽ chồng lên nhau theo trục. Vì vậy số liên kết pi sẽ là: 6 : 2 = 3
Một số tính chất chung của hydrocacbon thơm đã được liệt kê dưới đây.
- Các hợp chất này thể hiện tính thơm (ổn định bổ sung do cộng hưởng)
- Các hydrocacbon thơm không hòa tan trong nước.
- Tỷ lệ nguyên tử carbon so với nguyên tử hydro tương đối cao trong các loại phân tử này.
- Khi bị đốt cháy, các hydrocacbon thơm tạo ra ngọn lửa đỏ mạnh và có muội than ám trong khói đen.
- Các hợp chất này thường trải qua phản ứng thế thơm điện di và phản ứng thế nhân thơm.
Có thể lưu ý rằng các hợp chất hidrocacbon thơm này có thể là đơn vòng hoặc đa vòng.
Các phản ứng của Hydrocacbon thơm
Nhiều phản ứng hóa học hữu cơ liên quan đến việc sử dụng hydrocacbon thơm làm chất phản ứng chính. Một số phản ứng như vậy được liệt kê trong tiểu mục này cùng với mô tả ngắn gọn về từng phản ứng này.
1. Phản ứng thế nhân thơm
Những phản ứng này liên quan đến việc thay thế một nhóm thế trên vòng của hydrocacbon thơm, thường là nguyên tử hydro bằng một nhóm thế khác.
Các loại phổ biến của phản ứng thay thế thơm bao gồm:
- Phản ứng thế nhân thơm
- Phản ứng thế thơm điện di
- Phản ứng thế nhân thơm gốc tự do
Phản ứng thế thơm là sự thay thế điện di được trình bày rất chi tiết tại bài viết: phản ứng thế thơm điện di của toluen
2. Phản ứng khớp nối
Trong các loại phản ứng này, sự kết hợp của hai mảnh có bản chất triệt để đạt được với sự trợ giúp của chất xúc tác kim loại. Khi các hydrocacbon thơm trải qua các phản ứng liên kết, loại liên kết sau đây có thể được hình thành.
- Liên kết cacbon-cacbon có thể được hình thành từ các phản ứng ghép cặp của arene và các sản phẩm như vinyl arene, alkyl arene, v.v. được hình thành.
- Sự hình thành các liên kết carbon-oxy có thể xảy ra trong các phản ứng này, tạo thành các hợp chất aryloxy.
- Liên kết carbon-nitơ có thể hình thành trong các phản ứng ghép đôi, tạo ra các sản phẩm như anilin.
Có thể quan sát thấy một ví dụ về phản ứng kết đôi liên quan đến hydrocacbon thơm trong quá trình aryl hóa perfluorobenzene, như minh họa bên dưới.
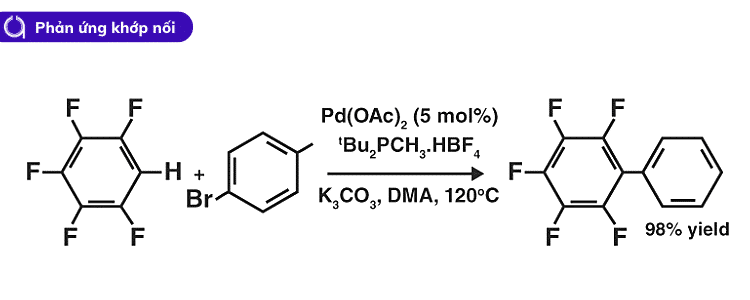
Chất xúc tác được sử dụng trong phản ứng này là Palladi(II) axetat. Cũng có thể lưu ý rằng DMA là tên viết tắt của Dimethylacetamide.
3. Phản ứng hydro hóa
Các phản ứng hydro hóa liên quan đến arene thường dẫn đến sự hình thành các vòng bão hòa. Một ví dụ về phản ứng như vậy là khử 1-naphtol thành hỗn hợp chứa các đồng phân khác nhau của decalin-ol.
Một ví dụ khác về phản ứng như vậy là phản ứng hydro hóa resorcinol với sự trợ giúp của niken xốp (còn được gọi là niken Raney) và dung dịch NaOH. Phản ứng này tiến hành thông qua sự hình thành của một enolate, và sự alkyl hóa liên tiếp của enolate này (với metyl iodua) để tạo ra 2-metyl-1,3-cyclohexanedione.
Công dụng của Hydrocacbon thơm

Việc sử dụng hydrocacbon thơm là phổ biến trong cả quá trình sinh học và tổng hợp. Một số công dụng của hydrocarbon thơm được liệt kê dưới đây.
- Sắc tố xanh được tìm thấy trong thực vật, thường được gọi là chất diệp lục, bao gồm các hydrocacbon thơm và rất quan trọng trong quá trình sản xuất thức ăn ở thực vật.
- Các axit nucleic và axit amin trong cơ thể con người cũng bao gồm các hydrocacbon thơm này.
- Methylbenzene là một hydrocarbon thơm được sử dụng làm dung môi trong keo mô hình.
- Naphtalen là nguyên liệu quan trọng trong sản xuất băng phiến.
- Để tổng hợp thuốc, thuốc nhuộm và chất nổ, một aryl hydrocarbon được gọi là Phenanthrene được sử dụng.
- Trinitrotoluene hoặc TNT là một hydrocarbon thơm rất quan trọng được sử dụng rộng rãi cho mục đích nổ.
- Ngành nhựa và công nghiệp hóa dầu sử dụng rộng rãi các hydrocacbon thơm.
Hiđrocacbon thơm đa vòng
Đây là những hydrocacbon bao gồm các vòng thơm ở dạng hợp nhất. Arenes tùy thuộc vào số lượng vòng benzen hợp nhất được phân loại thành:
- Cấu trúc vòng đơn: Benzen.
- Cấu trúc vòng kép: Naphtalen.
- Cấu trúc vòng ba: Antraxen.
Hydrocacbon thơm đa vòng có thể được tìm thấy trong than đá, hắc ín, dầu và một số thực phẩm nấu chín như cá hun khói, bánh mì nướng cháy, v.v.
Một ví dụ phổ biến của các hydrocacbon đa vòng này là naphtalen. Các hợp chất này được cho là chất gây ô nhiễm.
Một số ví dụ về hydrocacbon thơm là Methylbenzene, Naphthalene, Phenanthrene, Trinitrotoluene và o-dihydroxybenzene.
Câu hỏi thường gặp – FAQs
Hiđrocacbon nào là hiđrocacbon thơm?
Hydrocacbon thơm, thường được gọi là arenes, là các phân tử hữu cơ thơm được tạo thành hoàn toàn từ cacbon và hydro. “Vòng benzen” được đặt tên theo hydrocacbon thơm đơn giản nhất là benzen (C6H6). Hoặc có thể là nhóm phenyl (C6H5) còn được gọi là vòng benzen thiếu một nguyên tử hydro có thể được thay thế bởi một số nguyên tố khác (ví dụ các nguyên tốt thuộc nhóm Halogen) hoặc nhóm chức khác (ví dụ metyl CH3).
Kể tên một số Hiđrocacbon thơm thường gặp?
Một vòng thơm duy nhất tạo nên các hydrocacbon thơm đơn vòng (MAHs). Các hydrocacbon thơm dễ bay hơi và dễ tan trong nước nhất bao gồm benzen, toluen, etylbenzen và xylen (BTEX), là những chất gây ô nhiễm môi trường nổi tiếng.
Phản ứng thế thơm là gì?
Phản ứng thế vòng thơm điện di xảy ra khi một điện di thay thế một nguyên tử kết nối với vòng thơm trong một quá trình hữu cơ. Sự thay thế một nguyên tử hydro từ vòng benzen bằng một điện di là phổ biến trong các phản ứng này.
Làm thế nào để các hợp chất thơm phản ứng?
Các hợp chất thơm, còn được gọi là arenes, trải qua các phản ứng thế trong đó hydro thơm được thay thế bằng chất ái điện, dẫn đến sự thay thế chất ái điện. Liên kết chéo kim loại, chẳng hạn như phản ứng Suzuki, cho phép hai hoặc nhiều hợp chất thơm tạo ra liên kết cacbon-cacbon.
Giải thích phản ứng của Sandmeyer bằng một ví dụ là gì?
Phản ứng Sandmeyer là một phản ứng hóa học sử dụng muối đồng làm thuốc thử hoặc chất xúc tác để sản xuất aryl halogenua từ muối aryl diazonium. Một sự thay thế thơm gốc-nucleophilic là một ví dụ.
nguồn tham khảo wikipedia bài viết học thuật về Hydrocacbon thơm



